식약처 신규 연구사가 Gemini + NotebookLM으로 검토보고서 초안을 완성하기까지
NotebookLM 실습에 업로드할 심사보고서 5종과 교재 PDF를 내려받으세요.
※ 포함된 소스: 심사보고서_키트루다 · 심사보고서_엔허투 · FDA_Keytruda_Approval_Review_2014 · FDA_Keytruda_Label_2025 · 임상시험 위해성 평가 가이드라인

최신 동향을 파악하고 종합 보고서를 확보한다


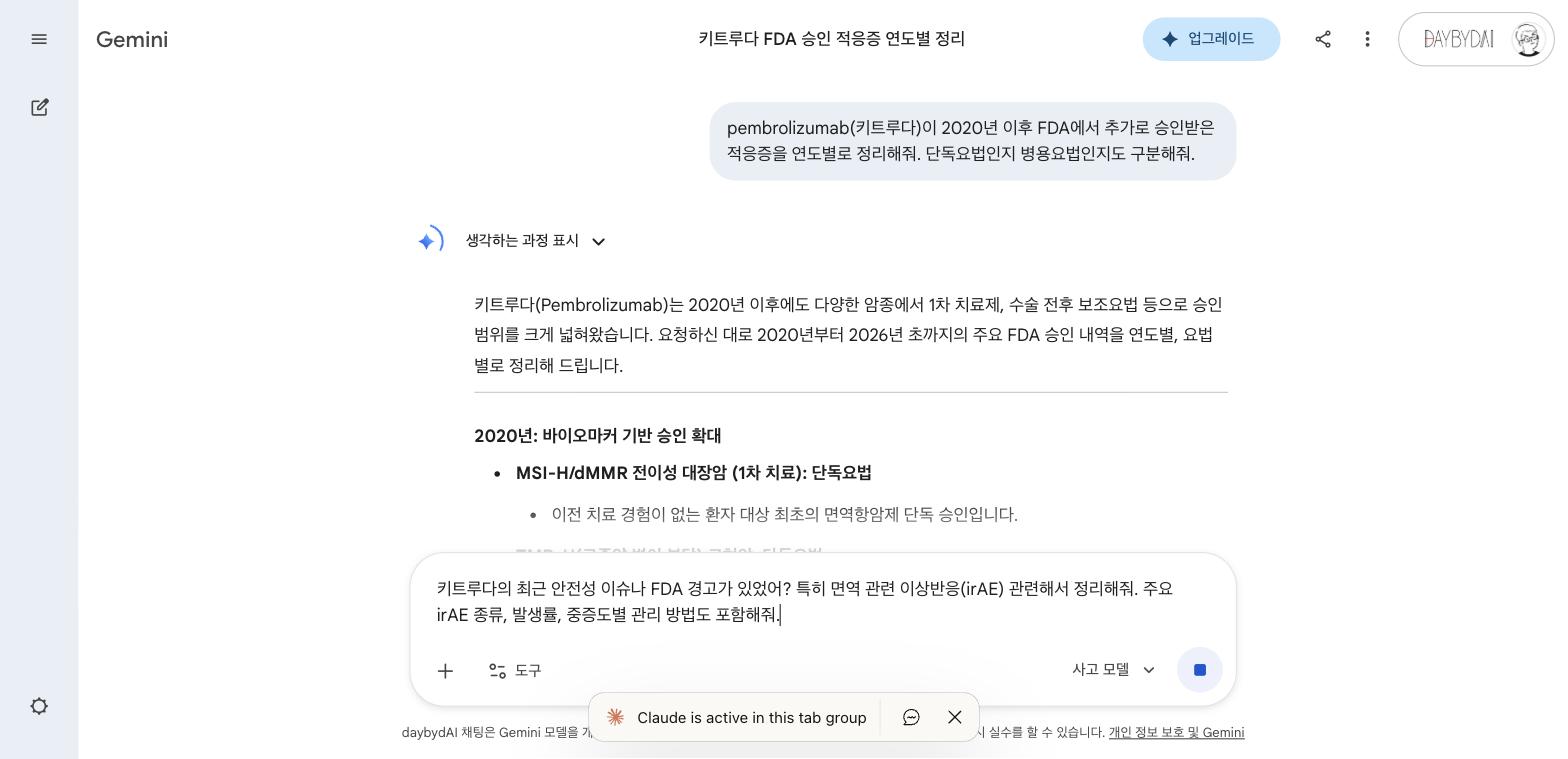
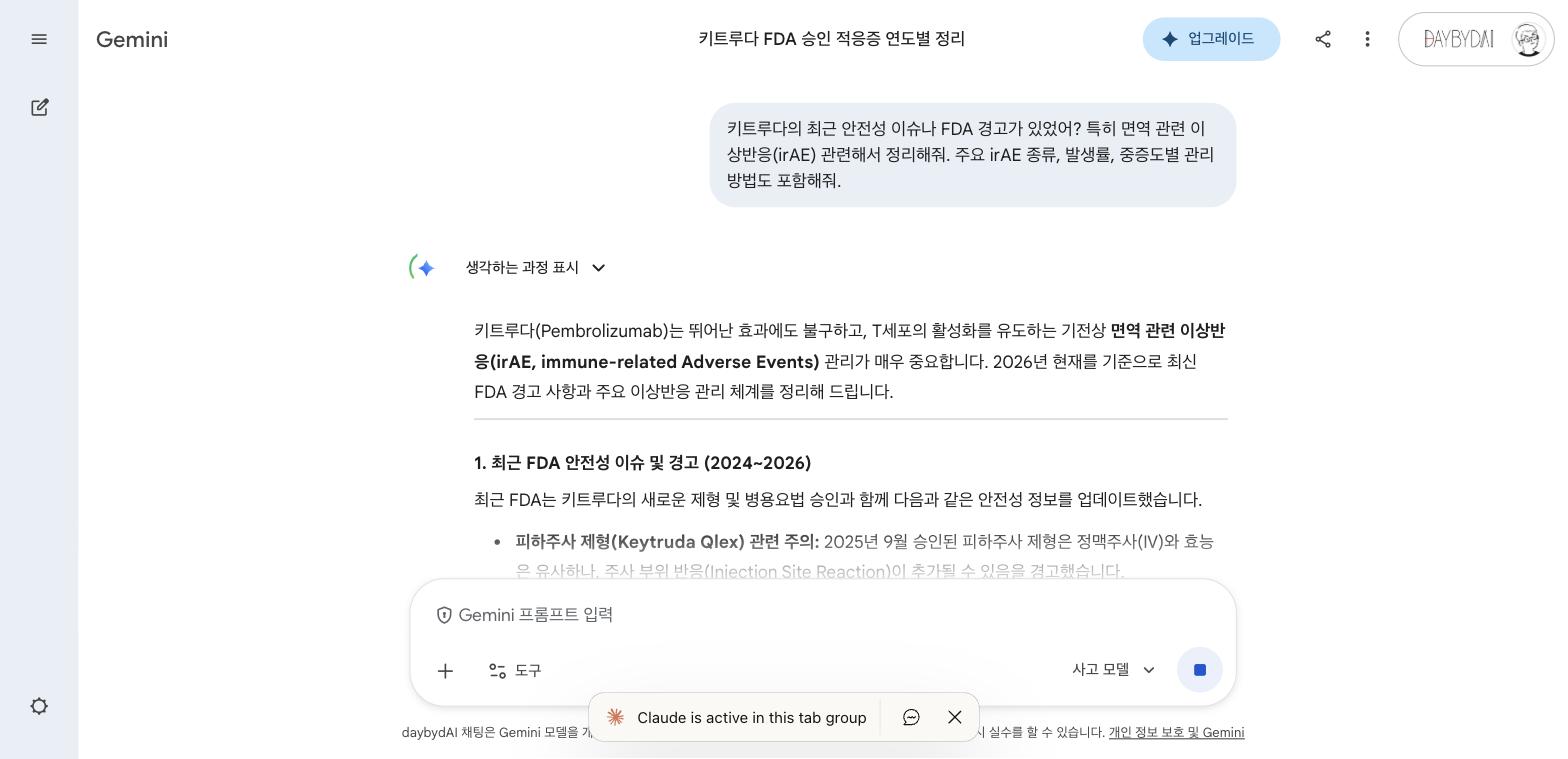





엔허투 양식 분석 → 키트루다 데이터 추출 → 초안 완성
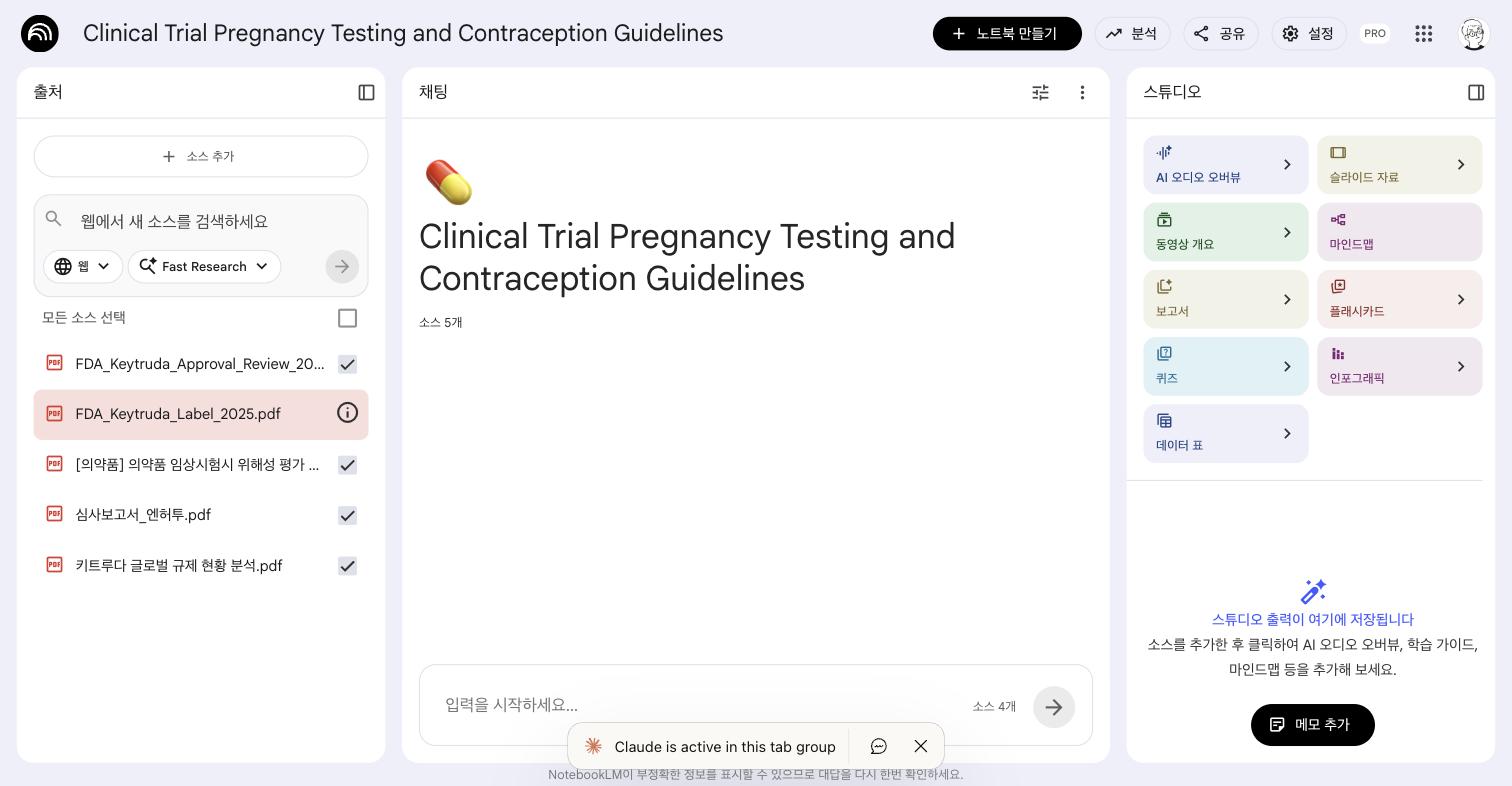
원인: Adobe Paper Capture Plug-in으로 생성된 스캔 PDF (169페이지, 9.9MB). 텍스트가 이미지로 저장되어 있어 NotebookLM이 OCR 처리에 실패.
대응: 딥리서치 결과에 2025 라벨 정보가 이미 포함되어 있어 대체 가능.
교훈: FDA accessdata에서 받은 파일이 스캔 버전인 경우가 있다. 실무에서도 자주 겪는 문제!

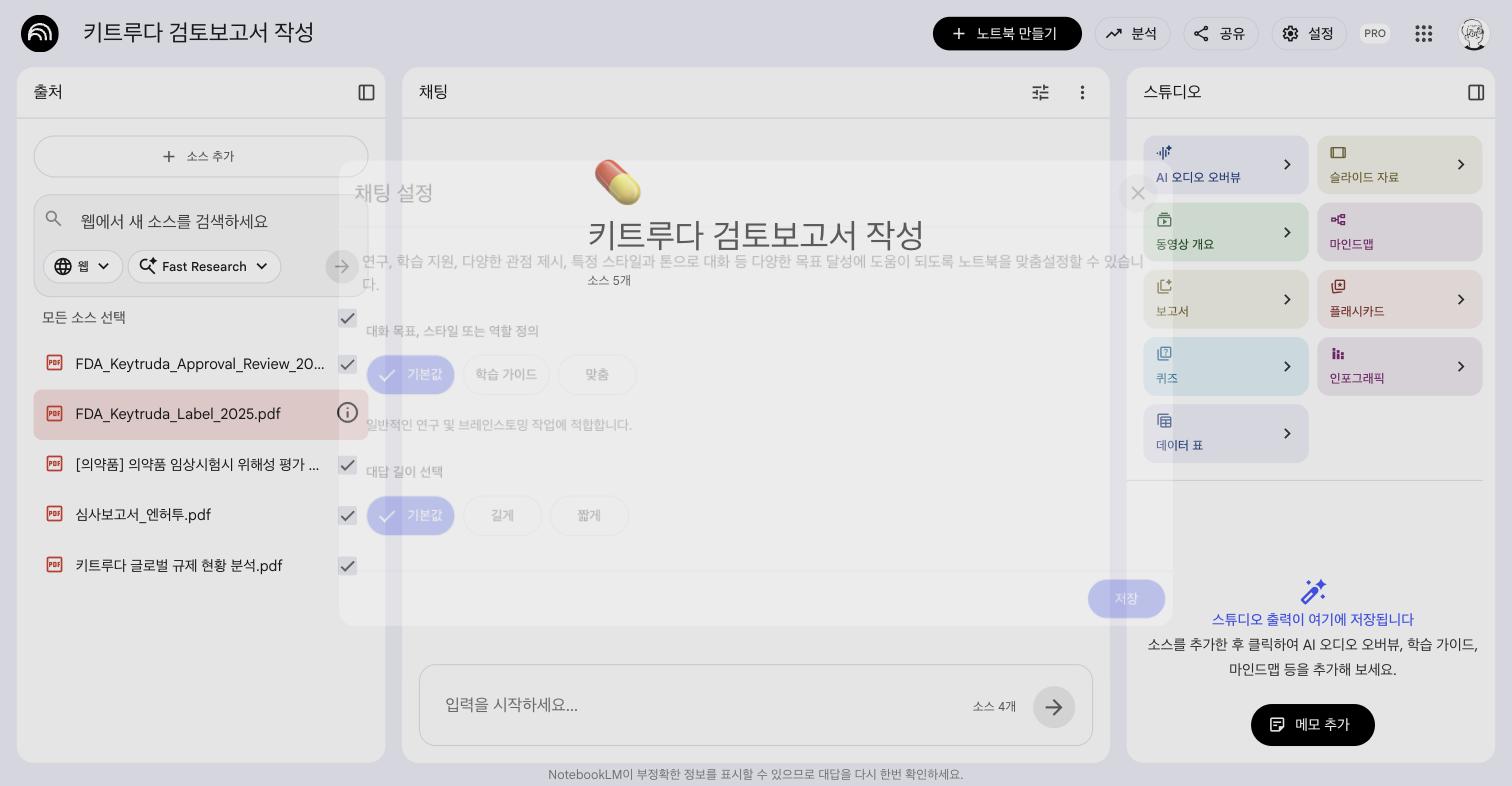
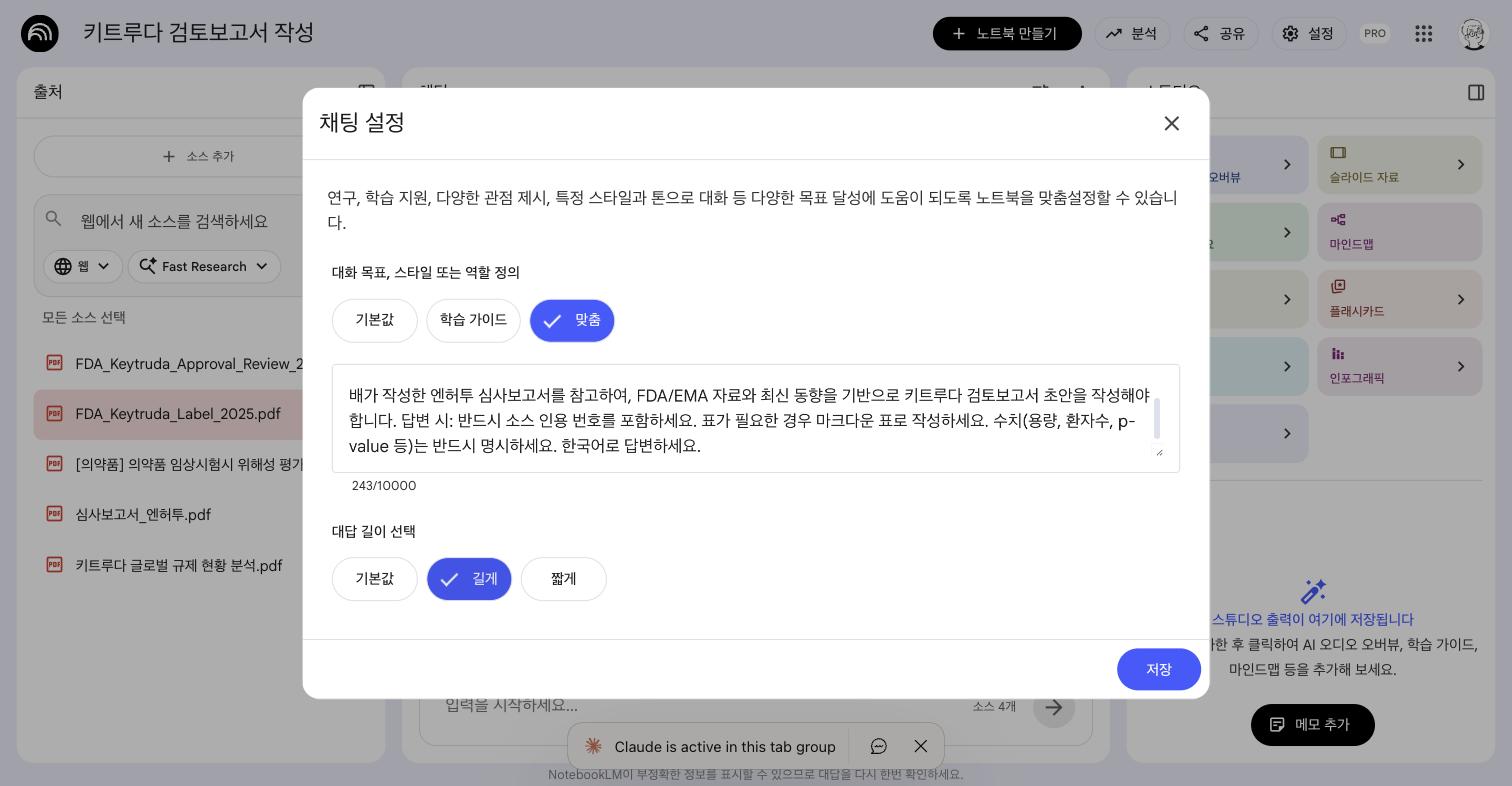
핵심 원칙: 이 단계에서는 심사보고서_엔허투.pdf만 선택해서 질문한다.
Q1: 전체 구조 분석
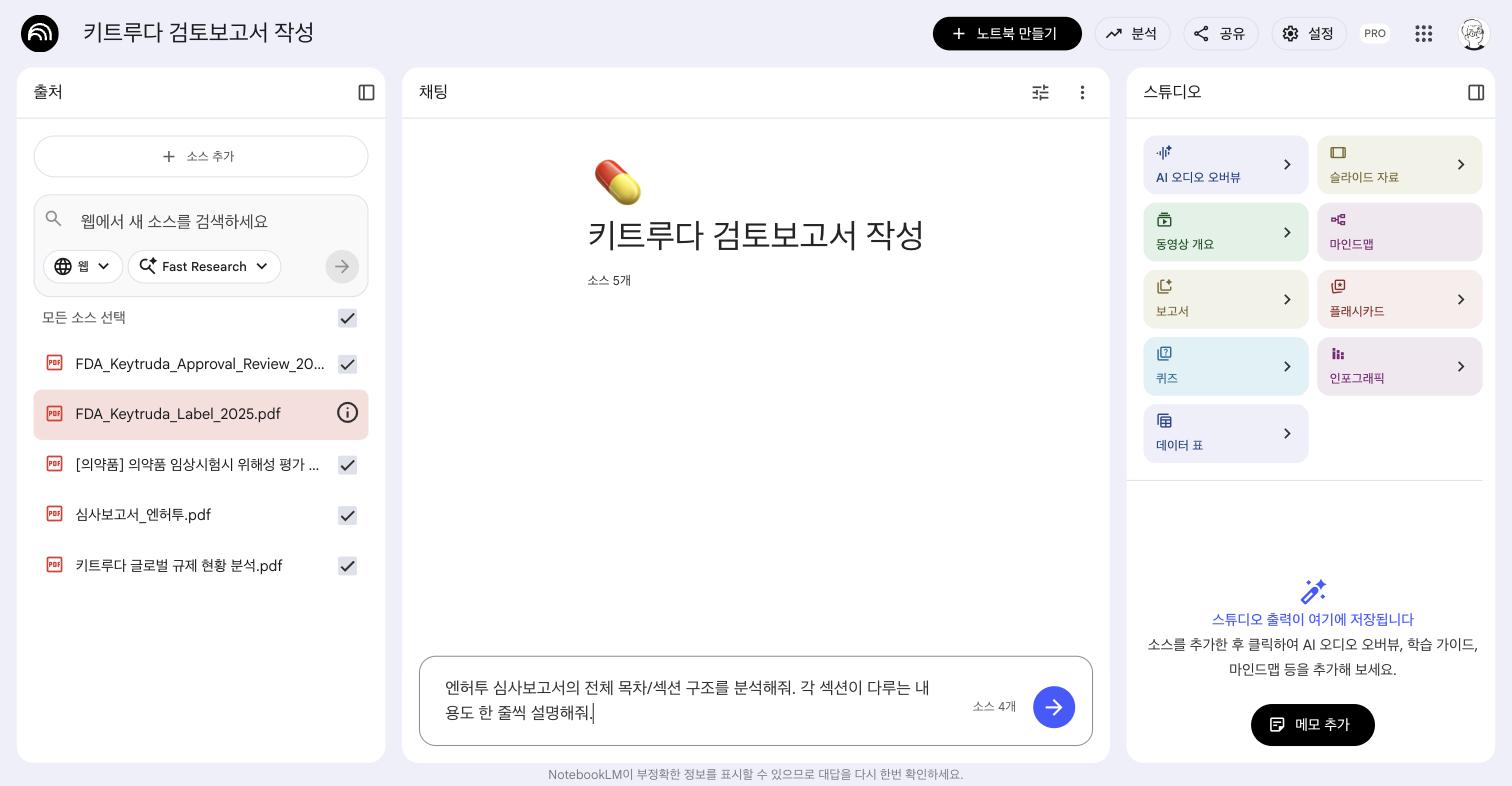
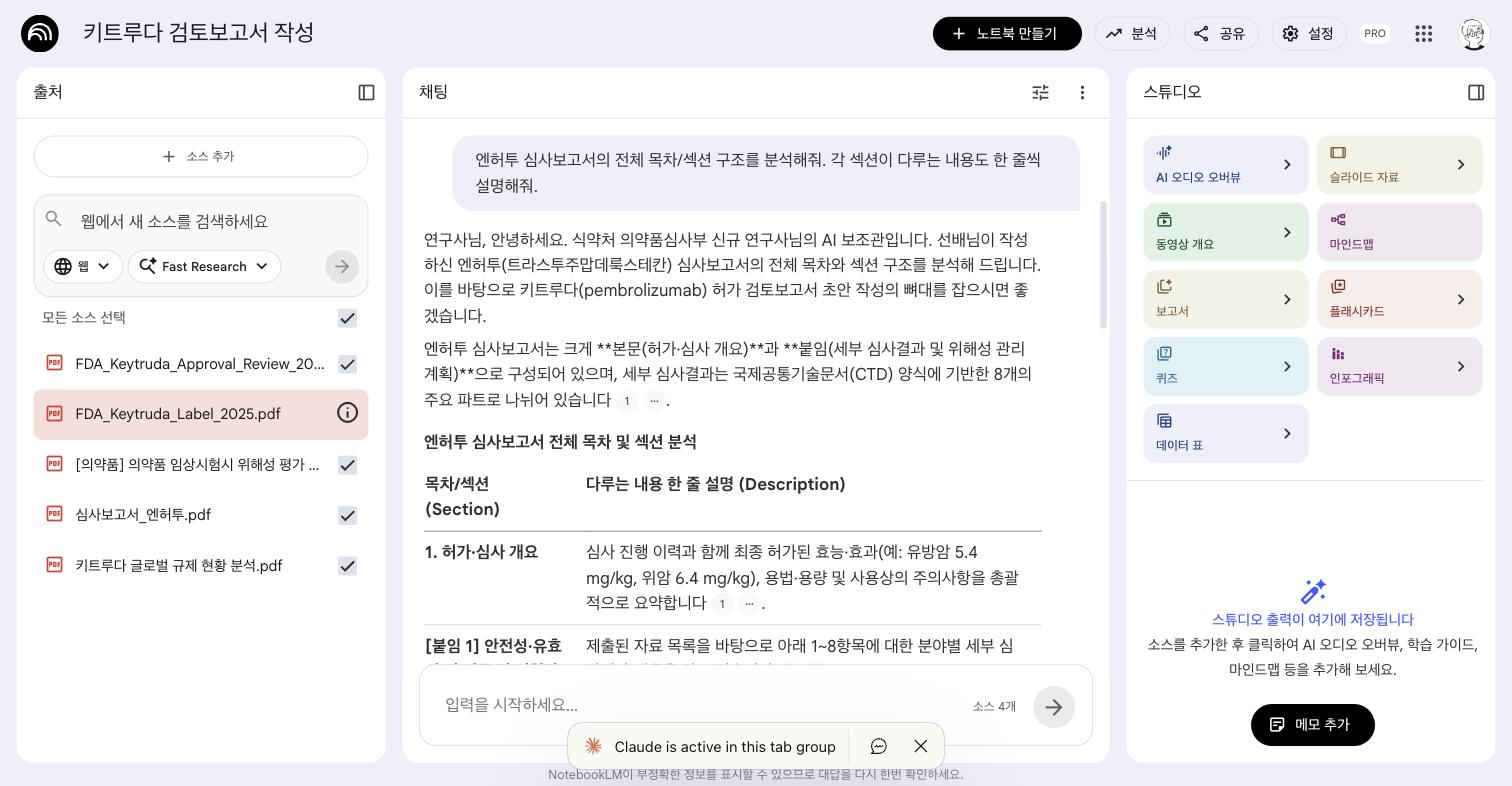
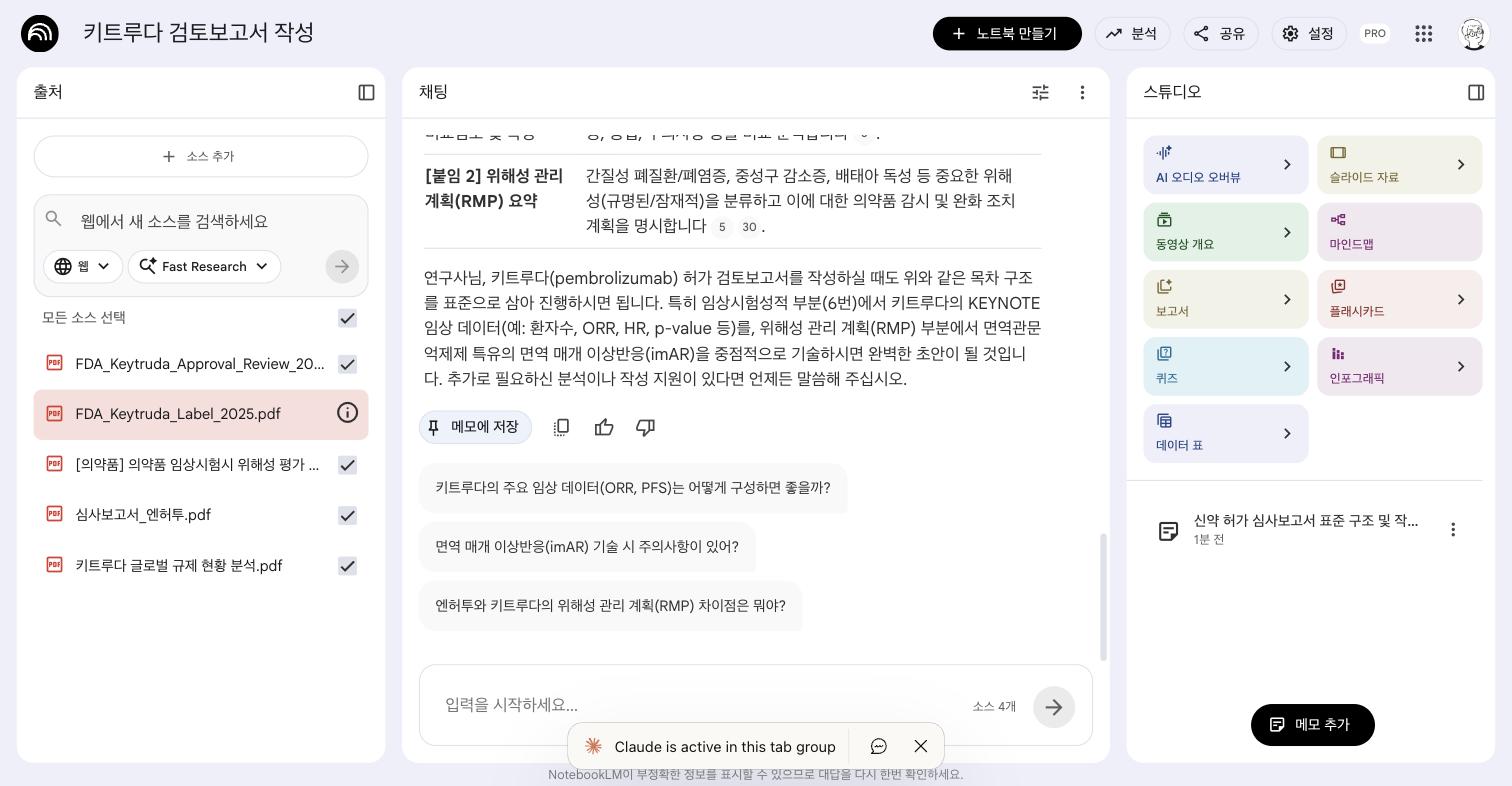

Q2: 해외 허가 현황 양식
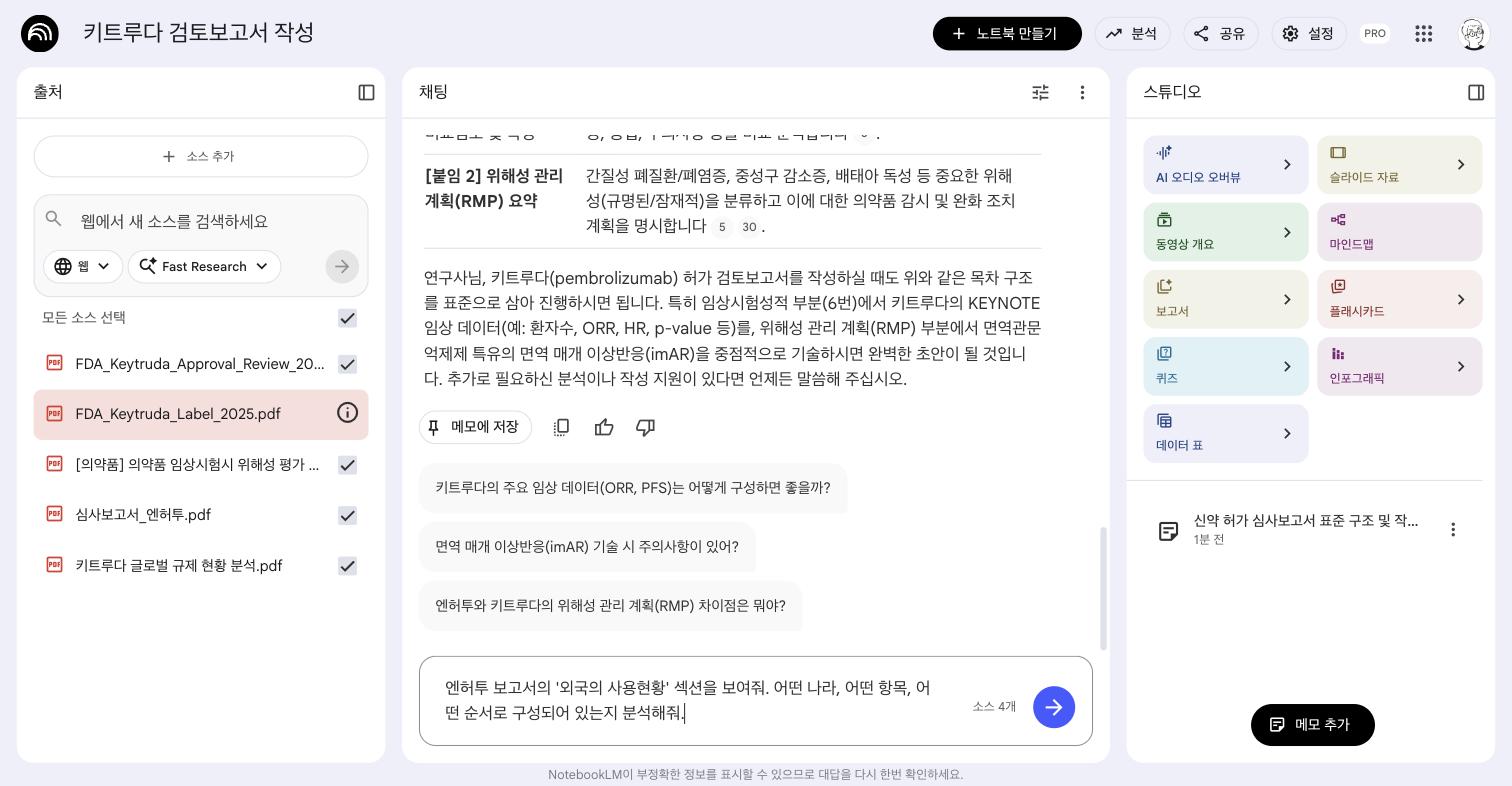

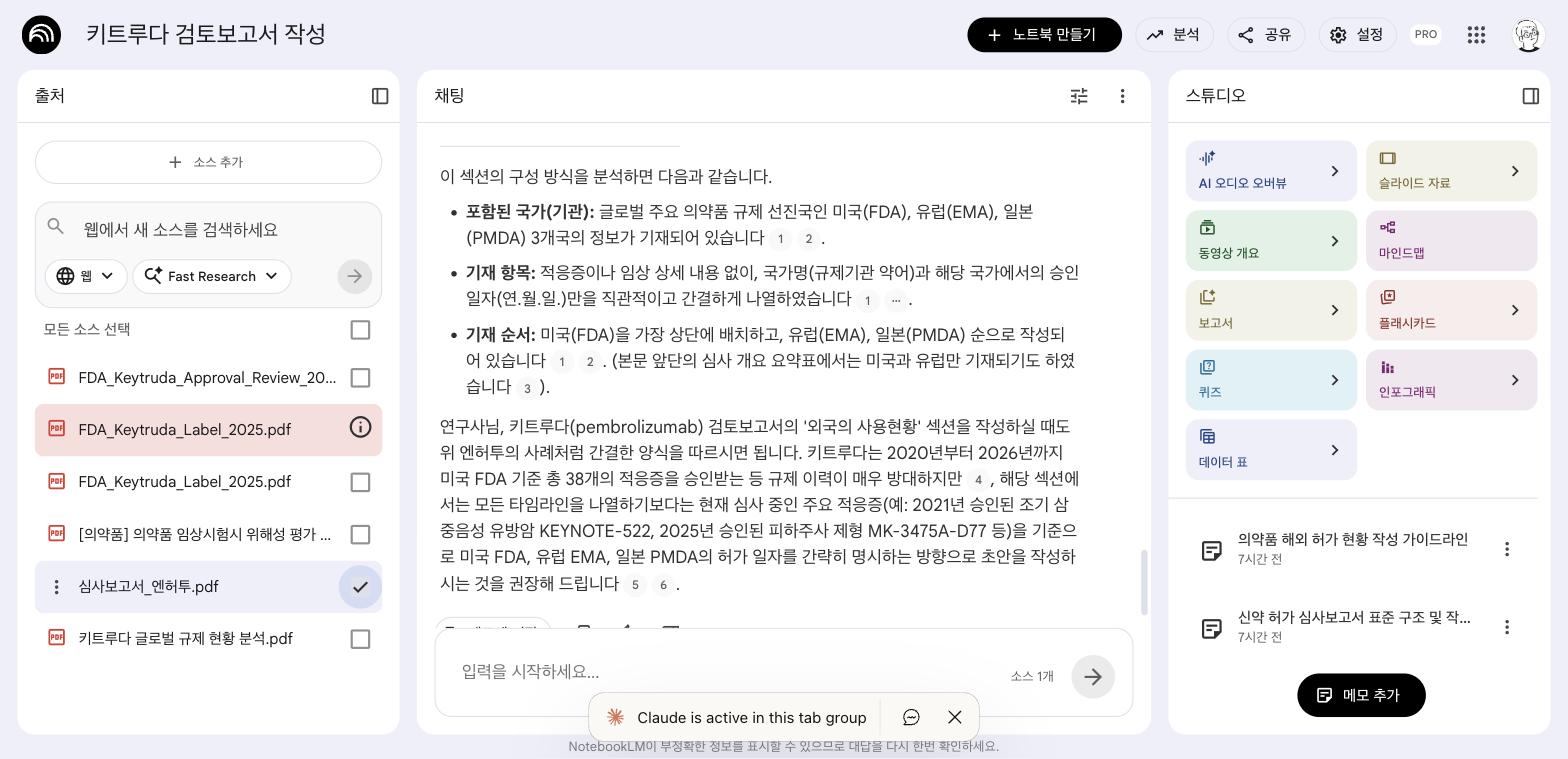

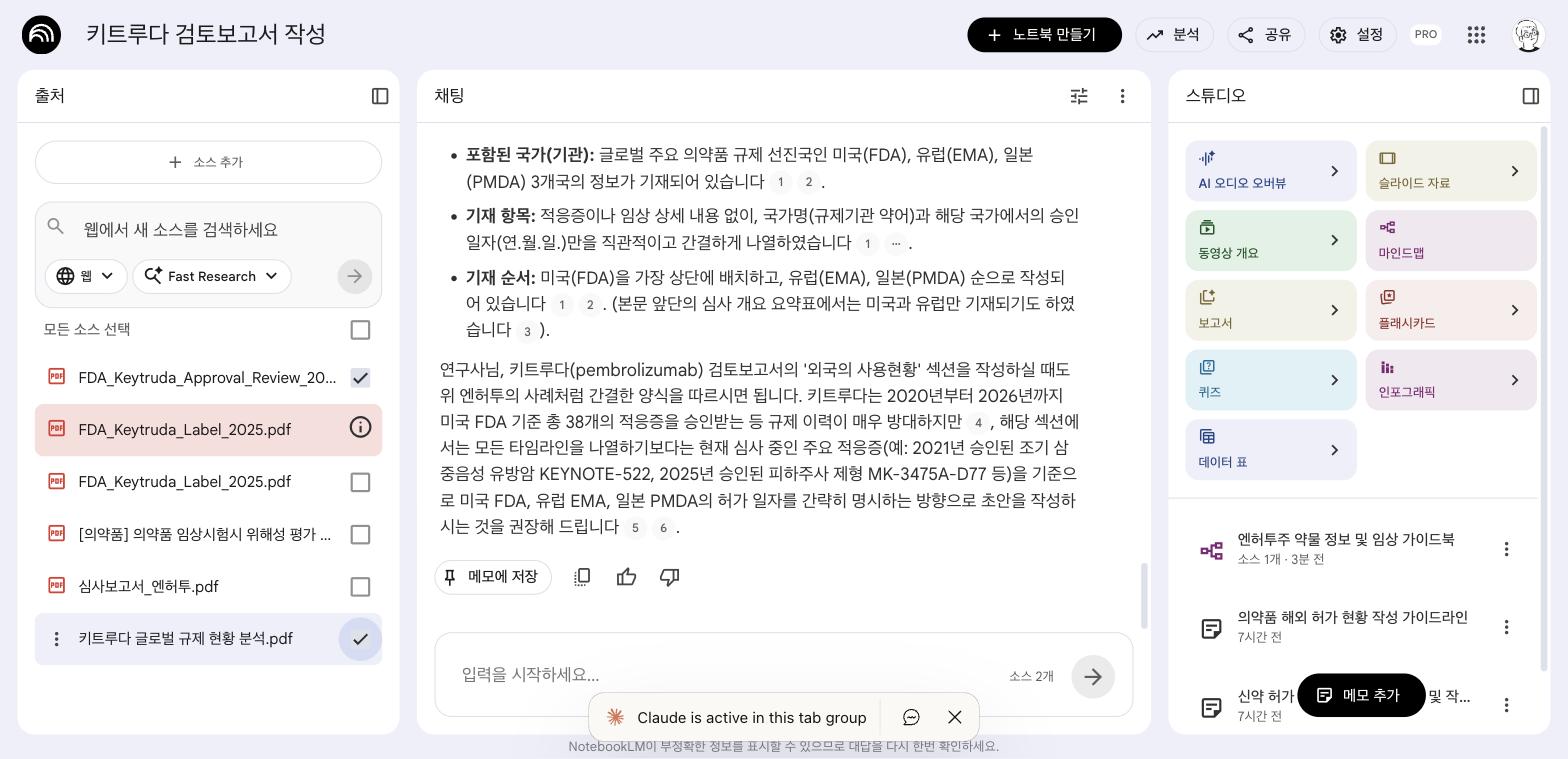
Q4: FDA 허가 정보
Q5: 유효성 데이터 표
Q7: 안전성 데이터


이전에 만든 노트들을 소스로 전환 → 전체 소스 선택 → 섹션별 초안 작성
Q9: 해외 허가 현황 초안
Q10: 유효성 검토 초안
Q11: 안전성 검토 초안
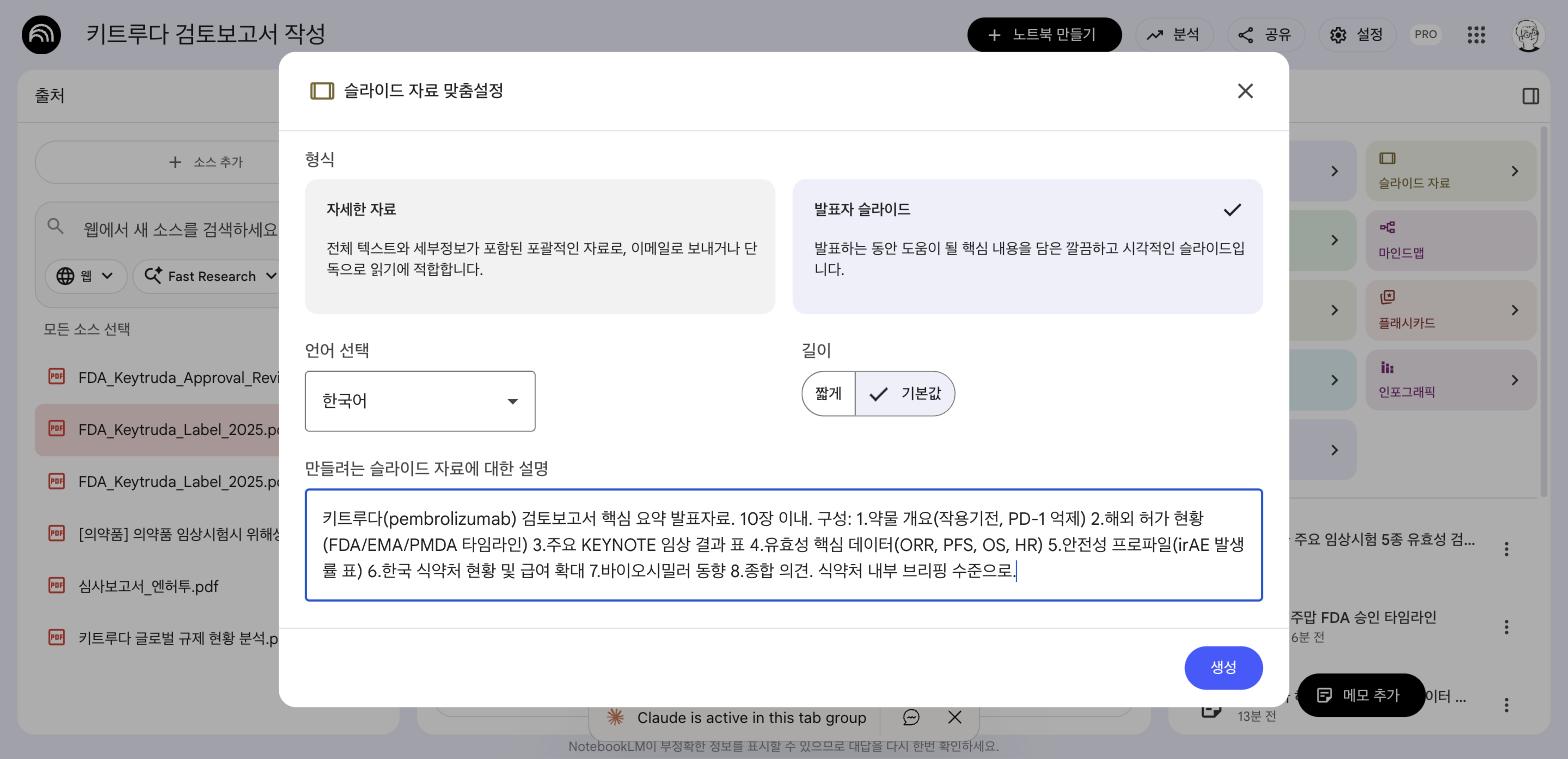
발표자 슬라이드
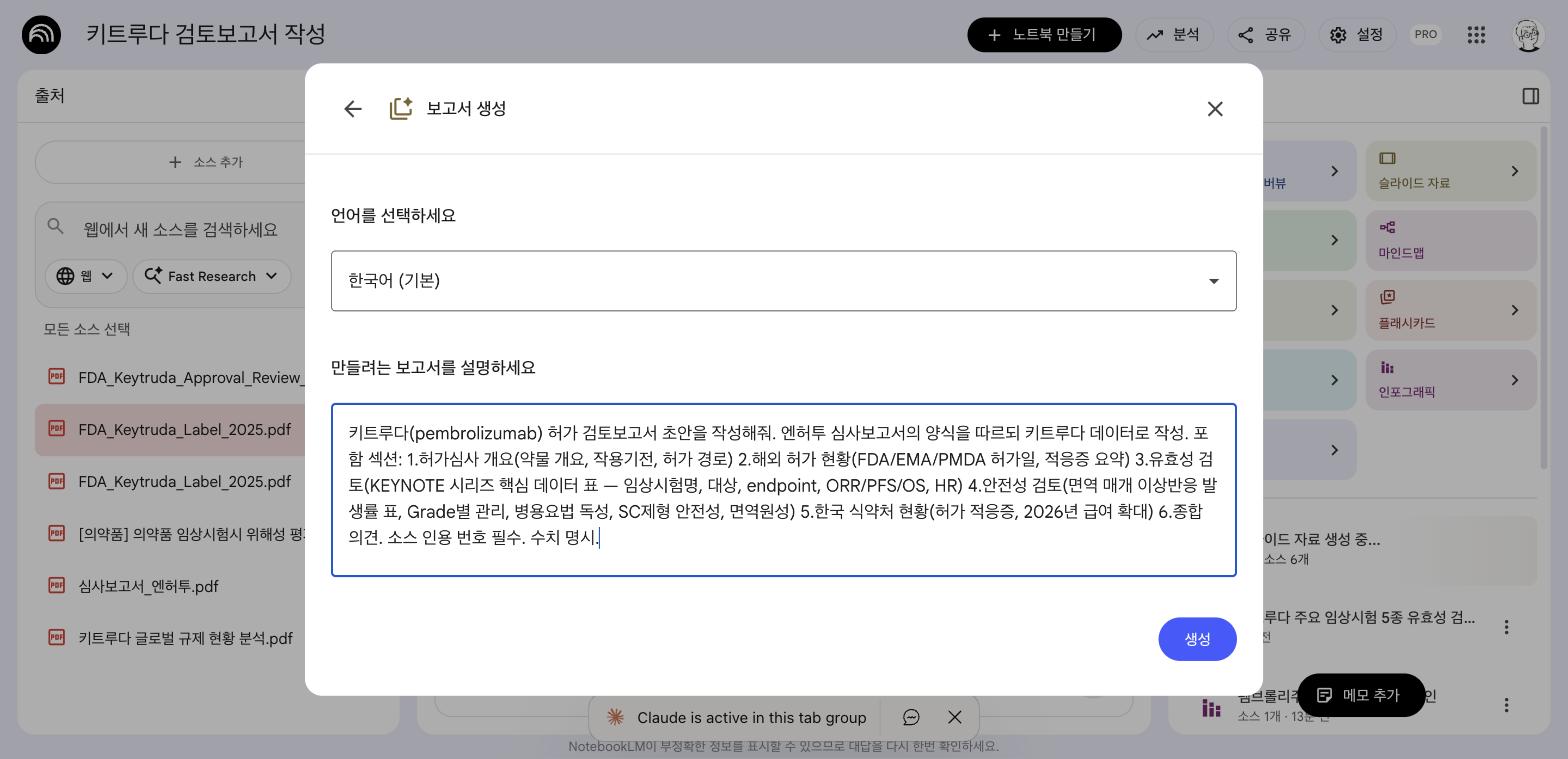
검토보고서 초안
| 종류 | 이름 | 소스 |
|---|---|---|
| 노트 7개 | Q1~Q11 답변 | 엔허투 구조, 해외허가, 유효성, 안전성, 초안 3종 |
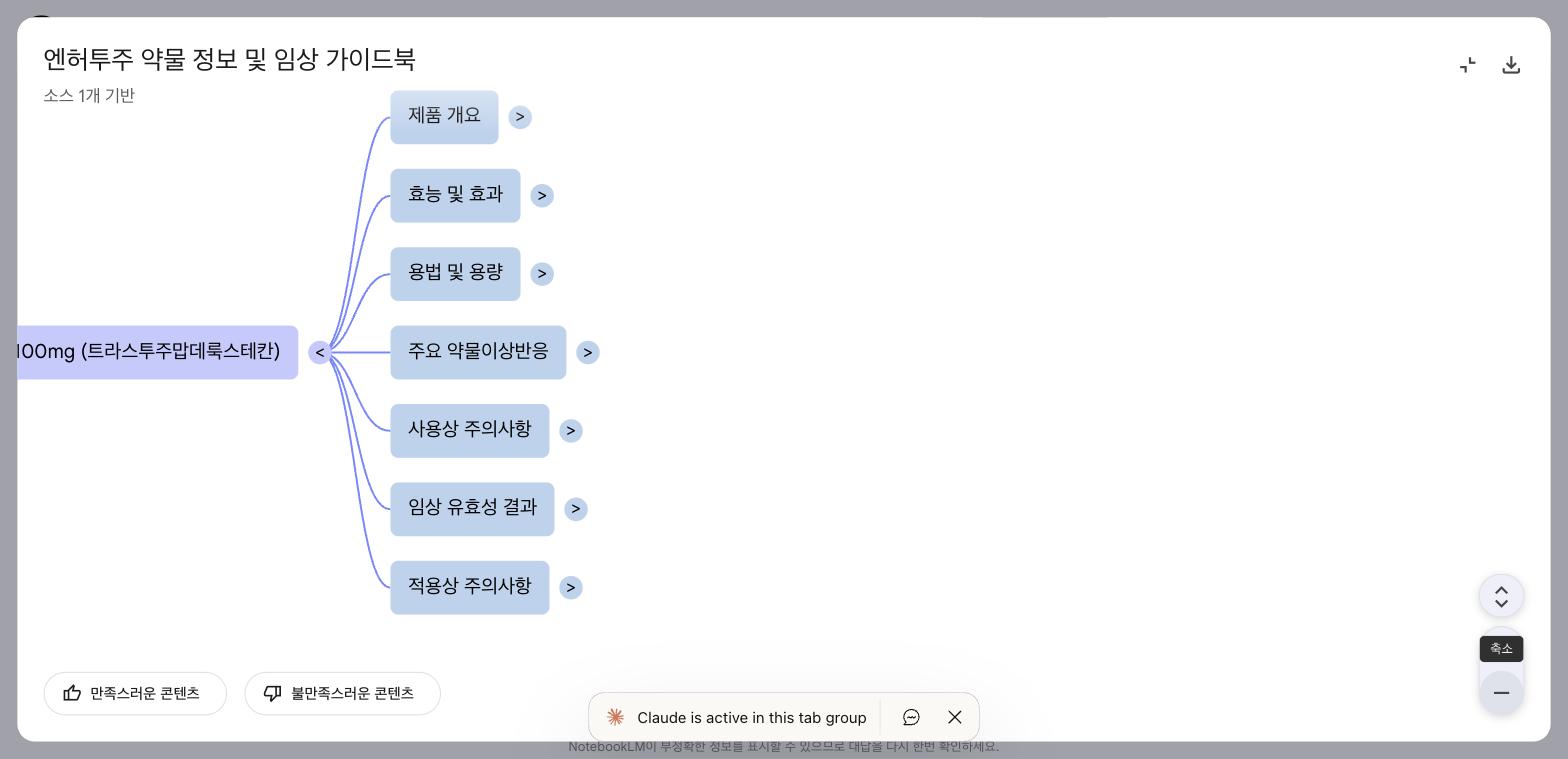
| 마인드맵 | 엔허투 약물 정보 | 엔허투 1개 |
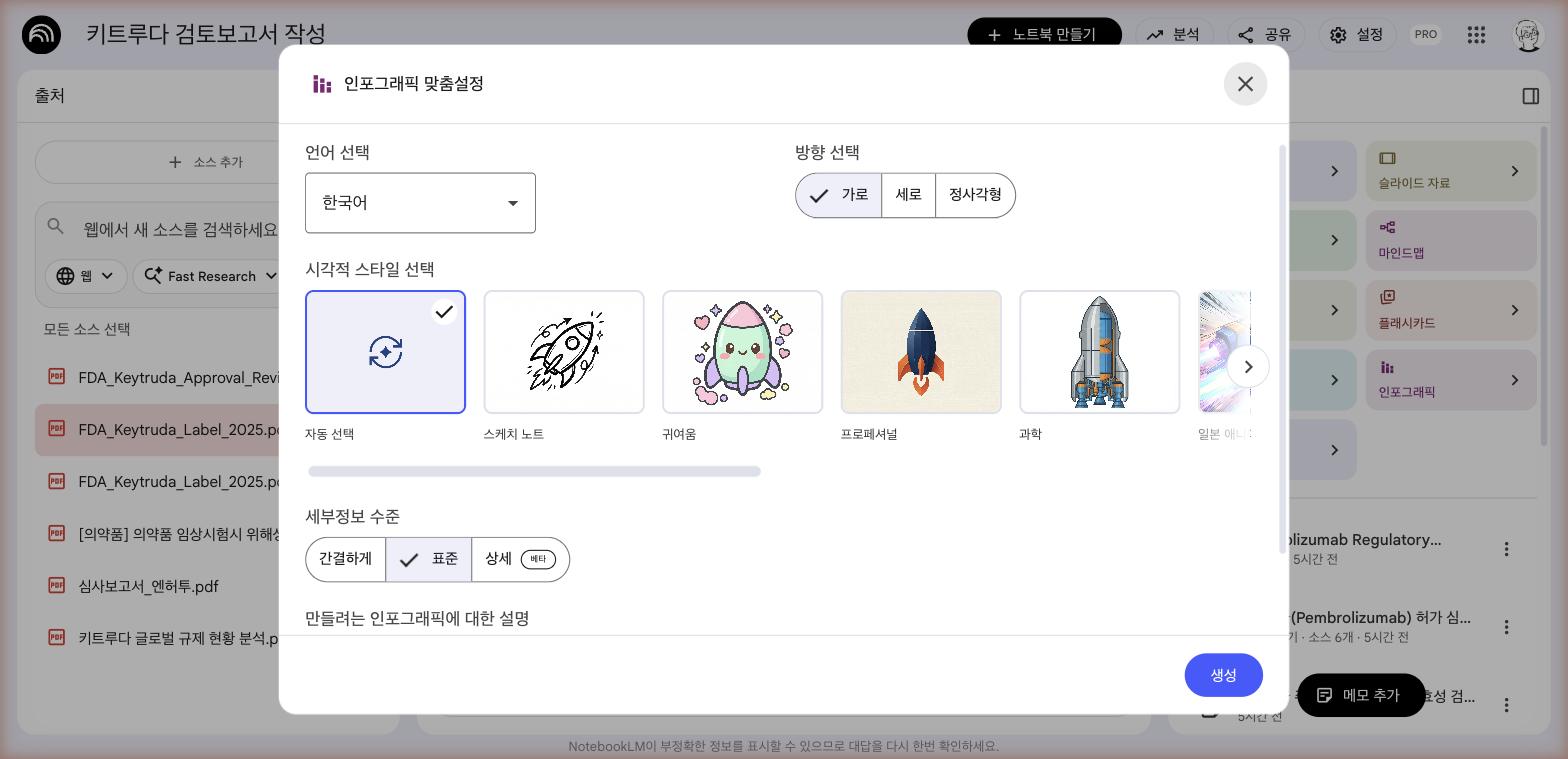
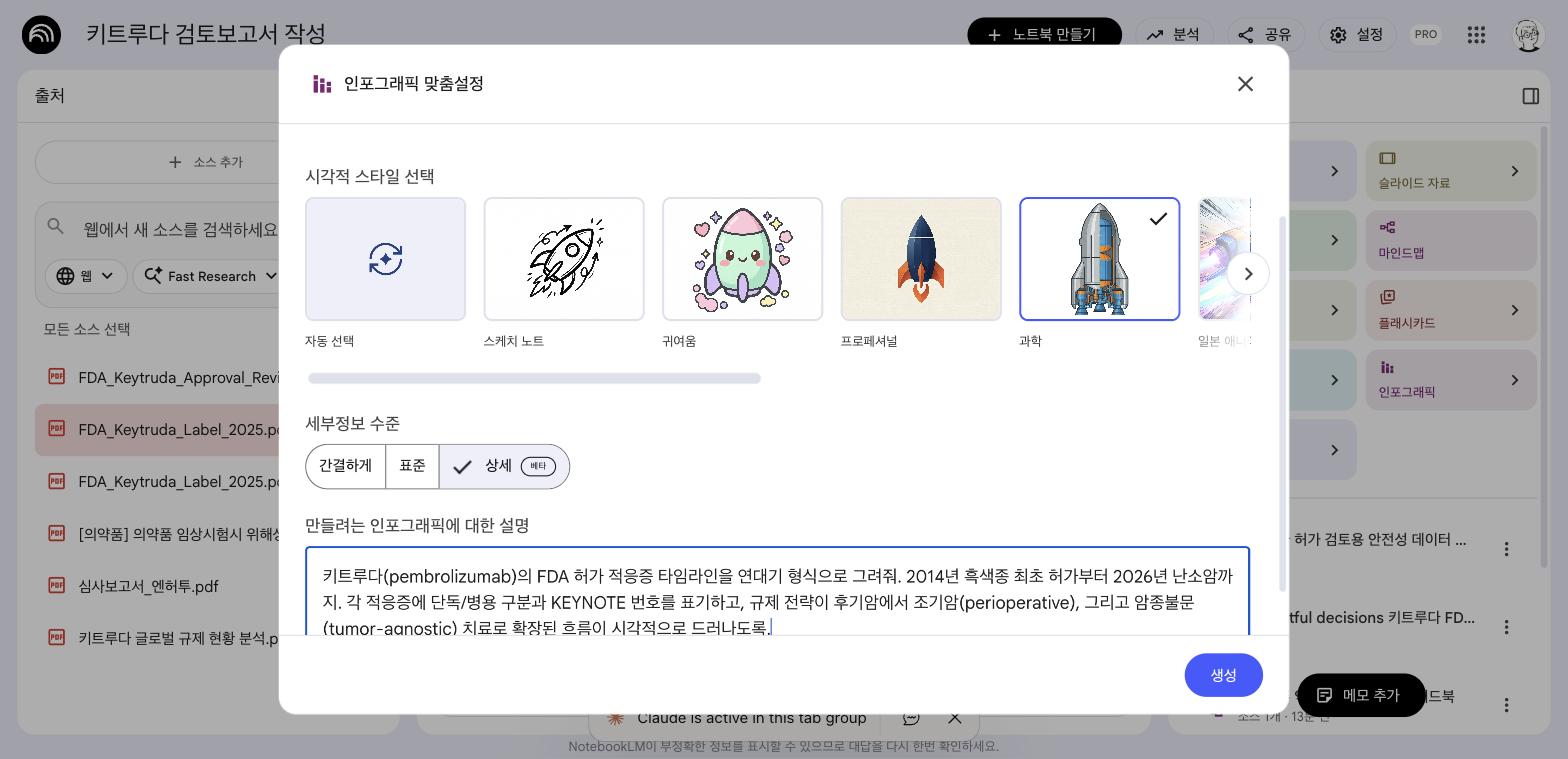
| 인포그래픽 | FDA 승인 타임라인 | 딥리서치 1개 |
| 슬라이드 | 검토보고서 브리핑 | 전체 6개 |
| 보고서 | 허가 심사 보고서 초안 | 전체 6개 |
AI 초안 vs 실제 심사보고서 — 뭐가 달랐나
1. 문서 유형이 다르다
| 항목 | AI 초안 | 실제 보고서 |
|---|---|---|
| 문서 유형 | 종합 검토보고서 (키트루다 전체) | 품목변경허가 보고서 (두경부암 추가 건) |

2. 국외 허가현황 분량이 다르다
| 항목 | AI 초안 | 실제 보고서 |
|---|---|---|
| 분량 | FDA/EMA/PMDA 타임라인 + 비교표 (수 페이지) | 딱 한 줄 |
| 내용 | 2014~2026 전체 적응증 | "미국(FDA): 2014.09.04. 최초 허가..." |

3. 안전성 데이터 깊이가 다르다
| 항목 | AI 초안 | 실제 보고서 |
|---|---|---|
| 안전성 표 | irAE 요약 표 (발생률 범위) | KEYNOTE별 개별 이상사례 표 |
| 임상검사치 | 거의 없음 | 별도 표 (고혈당증, ALT/AST 등) |
| 용량조절 | Grade별 원칙만 | 장기계통별 상세 표 |

| 항목 | 점수 | 한줄 평가 |
|---|---|---|
| 문서 구조 | 7/10 | 엔허투 양식 잘 따랐지만, 변경허가 구분 못함 |
| 유효성 | 8/10 | KEYNOTE 핵심 데이터 OK, 시험별 상세 표 부족 |
| 안전성 | 7/10 | irAE 분류/관리 OK, 임상검사치 부족 |
| 글로벌 분석 | 10/10 | 실제보다 훌륭 (딥리서치 성과) |
| 한국 현황 | 10/10 | 급여 확대 등 최신 정보 풍부 |
| 시각화 | 9/10 | 인포그래픽, 마인드맵 교재 수준 |
스캔 PDF(169p, 9.9MB)는 NotebookLM에서 처리 불가. ocrmypdf로 OCR 변환 필요.
마인드맵을 소스 5개 전부로 생성 → 부정확한 결과. 관련 소스만 선택하는 것이 핵심.
모델 드롭다운이 아니라 "도구" 버튼을 클릭해야 한다.
